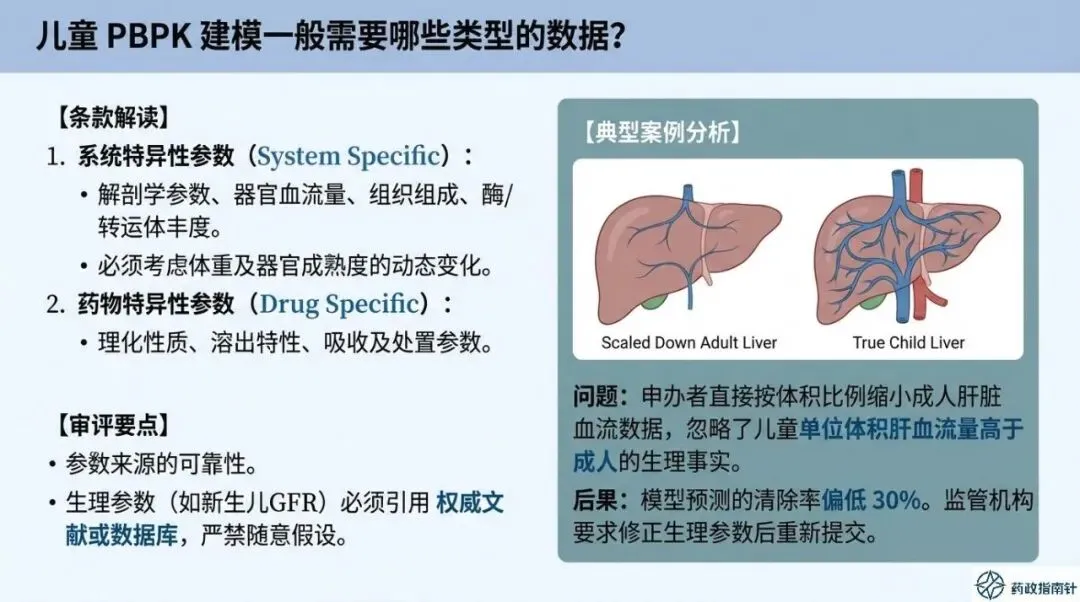
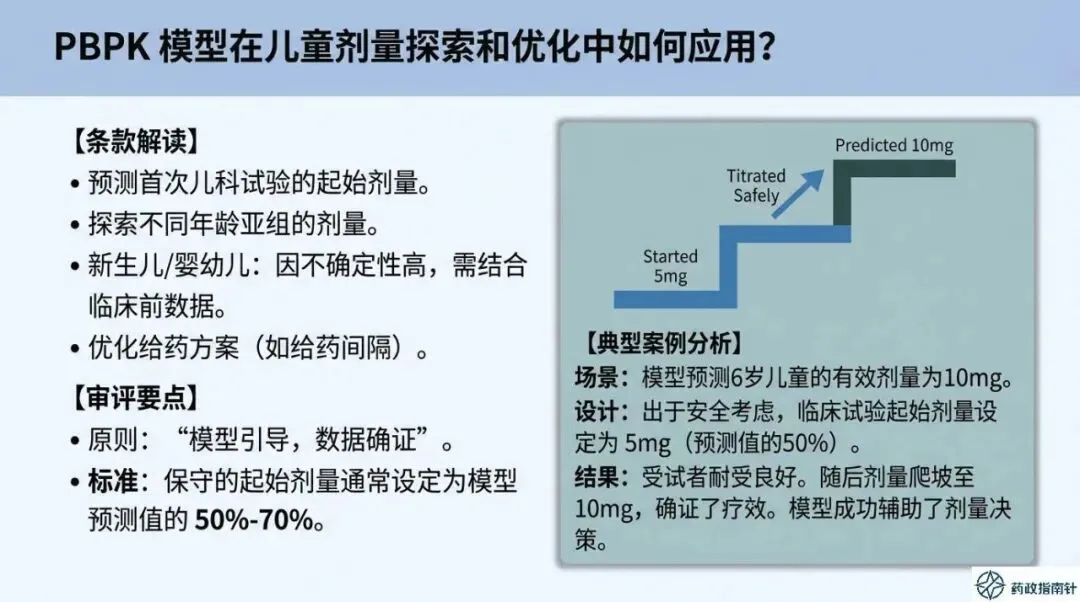
儿童用药安全与有效性一直是社会关注的焦点。为了更好地指导和规范儿童用药研发,国家药品监督管理局药品审评中心(CDE)2025年10月11日发布了《儿童用药研发常见/共性问题及一般性答复》,针对业内普遍关心的热点和难点问题进行了详细解答,共37个问题。这份文件分析了前15个问题,不仅涵盖了儿童参与者知情同意的特殊考量、各方职责界定等基础性问题,还深入探讨了因信息缺失带来的风险、风险管理计划(RMP)的应用、个例安全性报告(ICSR)和研发期间安全性更新报告(DSUR)的特殊要求 。特别值得一提的是,文件对生理药代动力学(PBPK)模型在儿童药物研发中的应用给予了高度关注,从一般策略、所需数据类型、潜在风险控制,到在剂量探索、优化、儿童用剂型开发中的应用,以及报告要求等方面都做了全面阐述 。此外,文件还就数据外推的前提、涉及的模型、安全性数据外推的注意事项以及如何选择合适的外推方法等问题提供了明确指导,旨在帮助研发机构更科学、高效地开展儿童用药研发工作 。



通过对上述15个常见问题的详细解读,我们可以清晰地看到,CDE发布的这份文件为我国儿童用药研发提供了一套更为清晰、具体的指导原则和操作指南 。从知情同意的伦理考量到临床试验中各方职责的明确,从安全性信息的评估与报告到风险管理计划的制定与实施,每一个环节都体现了对儿童受试者权益的优先保护和对药物研发科学性的严格要求 。特别是针对PBPK模型和数据外推等前沿技术方法的应用,文件不仅给予了充分的肯定和鼓励,也明确了其应用边界和注意事项,为这些技术在儿童用药研发中的规范应用奠定了坚实基础 。我们相信,随着这些指导原则的深入贯彻和实施,必将有力推动我国儿童用药研发水平的整体提升,为广大儿童患者带来更多安全、有效、适宜的治疗药物,更好地保障儿童群体的健康权益。同时,我们也期待未来能有更多关于儿童用药研发的指导性文件出台,不断完善相关政策法规体系,为儿童用药研发创造更加有利的环境。