氯气在水溶液中溶解性的影响因素的探究PPT
- 2026-05-20 12:57:19

“文武之道HX”是湖北黄冈黄老师个人公众号,旨在传播个人教学资料和资源,公众号坚持分享个人汇编、组编和自编的精品资料,号内所有资源均可下载,但时间有限定,希望您第一时间下载!您若觉得资源好,请帮忙转发并分享到朋友圈,让更多的的人看到,谢谢!!
致各位读者:因公众号平台改变了推送规则,如果想正常看到“文武之道HX”的推送,可能需要大家在阅读后,在文末右下角点一下“在看”或者“星标”,我们每次的新文章才会第一时间出现在你的订阅列表里,人海茫茫,不想和大家错过。分享课件下载请及时,超过期限需要资料需付费领取。具体操作只有四步:
(1)点击文章标题下面的蓝字“文武之道HX”或下面名片
(2)点击手机右上角的“…”
(3)选择“设为星标“
(4)找到关键词,点击发消息,手动输入关键词
1. 利用如图所示装置及药品完成实验,能达到实验目的的是
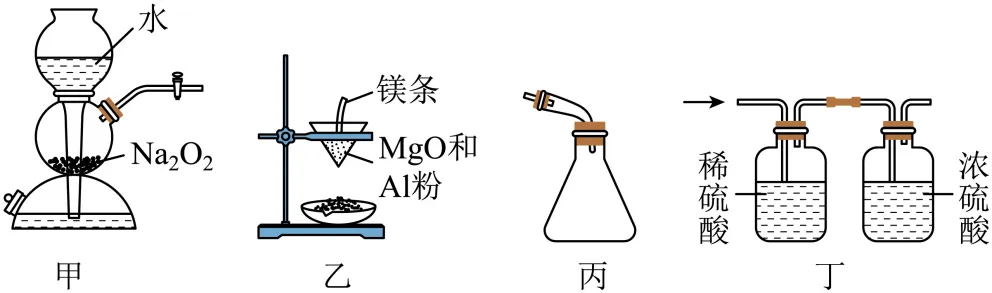
A. 用装置甲制取O2B. 用装置乙制备金属镁
C. 用装置丙作为蒸馏的接收装置D. 用装置丁除去Cl2中混有的HCl并干燥
【答案】D
【解析】
【详解】A.Na2O2与H2O剧烈反应生成NaOH和O2,同时放出大量的热,Na2O2不是块状且难溶于水的固体,不能用启普发生器制备,故A错误;
B.Mg的金属活动顺序强于Al,不能通过铝热反应制备,故B错误;
C.蒸馏时,锥形瓶不能用瓶塞,故C错误;
D.稀硫酸中含有大量氢离子,可以抑制氯气的溶解,而稀硫酸中的水可以吸收HCl,洗气后再用浓硫酸干燥,可制得干燥的氯气,故D正确;选D。
2.常温下,向新制氯水中滴加少量烧碱溶液,溶液中含氯粒子的物质的量分数与溶液pH关系如图所示。
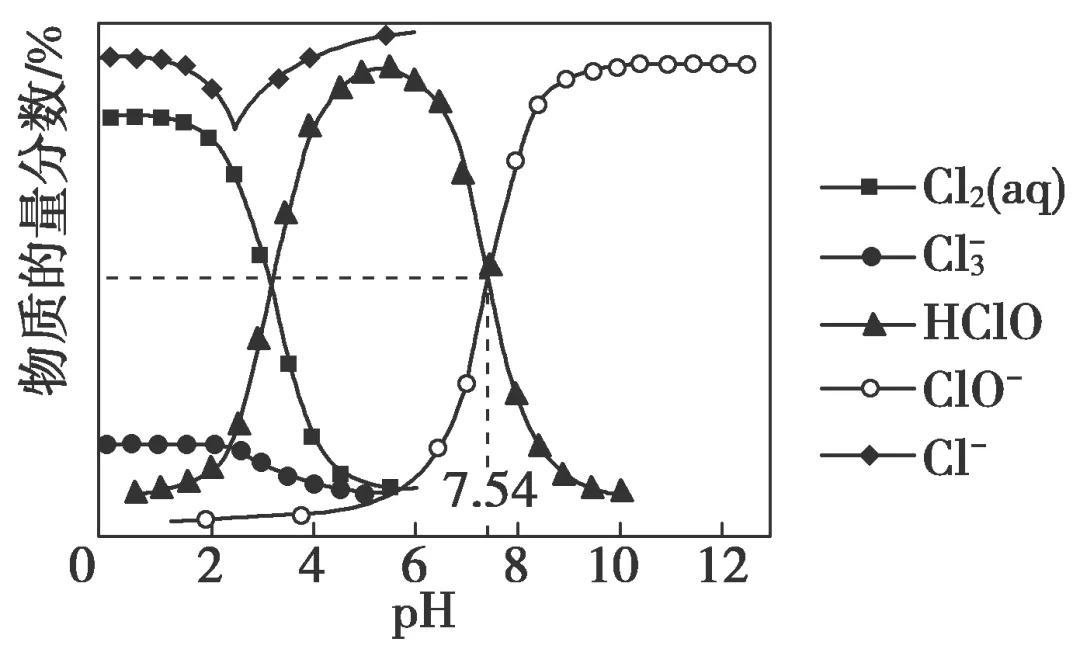
下列说法错误的是()
A.pH=2时,c(Cl-)>c(Cl2)>c(Cl3-)>c(HClO)>c(ClO-)
B.pH=5左右,溶液中c(HClO)最大,漂白效率最高
C.常温下,HClO电离常数(Ka)的数量级为10-7
D.中性溶液中存在:c(Na+)=c(HClO)+2c(ClO-)
解析:选C。观察、识别图像,pH=2时,c(Cl-)>c(Cl2)>c(Cl3)>c(HClO)>c(ClO-),A项正确;由题图可知,pH=5左右,溶液中c(HClO)最大,次氯酸浓度越大,漂白效率越高,B项正确;pH=7.54时,c(HClO)=c(ClO-),Ka=c(HClO)=1×10-7.54,数量级为10-8,C项错误;电荷守恒式为c(Na+)+c(H+)=c(OH-)+c(ClO-)+c(Cl3)+c(Cl-),中性溶液中c(H+)=c(OH-),再结合得失电子守恒c(Cl-)+c(Cl3)=c(HClO)+c(ClO-),可得c(Na+)=2c(ClO-)+c(HClO),D项正确。
3.(2022·黑龙江哈尔滨·哈九中校考模拟预测)相同温度和压强下,研究氯气分别在不同浓度的盐酸和氯化钠溶液中的溶解情况,实验测得氯气的饱和浓度c(Cl2)与盐酸和氯化钠溶液的浓度关系如图所示。
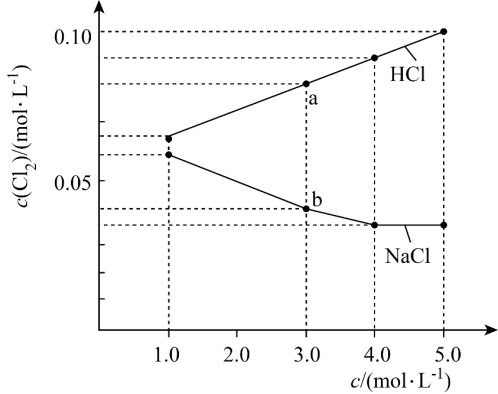
已知:氯气溶解过程发生如下反应:
①Cl2(aq)+H2O(l)⇌H+(aq)+Cl-(ag)+HClO(aq) K1=4.2×10-4
②Cl2(aq)+Cl-(aq)⇌Cl3-(aq) K2=0.19
③HClO(aq)⇌H+(aq)+ClO-(aq) Ka=3.2×10-8
下列说法正确的是
A.a点溶液中存在:c(H+)>c(Cl-)>c(ClO-)>c(Cl3-)
B.b点溶液中存在:c(H+)+c(Na+)<c(Cl-)+c(Cl3-)+c(ClO-)
C.由对比实验得出Cl-对Cl2的溶解存在较大的抑制作用
D.NaCl曲线中,随着Cl2溶解度的减小,溶液中增大
【答案】D
【详解】A.a点溶液中c(HCl)=3.0mol/L,c(Cl2)约为0.81mol/L,HCl为强电解质,完全电离,电离出的氯离子部分与Cl2结合生成Cl3-,所以c(H+)>c(Cl-)>c(Cl3-),K2>K1>Ka,所以c(Cl3-)>c(ClO-),综上所述c(H+)>c(Cl-)>c(Cl3-)>c(ClO-),A错误;
B.根据电荷守恒可知,b点溶液存在:c(H+)+c(Na+)=c(Cl-)+c(Cl3-)+c(ClO-)+c(OH-),
故c(H+)+c(Na+)>c(Cl-)+c(Cl3-)+c(ClO-),B错误;
C.HCl和NaCl溶液均能电离出Cl-,但在HCl溶液中,随着c(Cl-)增大,c(Cl2)增大,说明此时主要发生反应②,c(Cl-)增大使反应②平衡正向移动,促进氯气的溶解,C错误;
D.NaCl溶液中,=,随着Cl2溶解度的减小,反应①逆向移动,溶液中c(H+)减小,所以增大,即增大,D正确;
故选D。
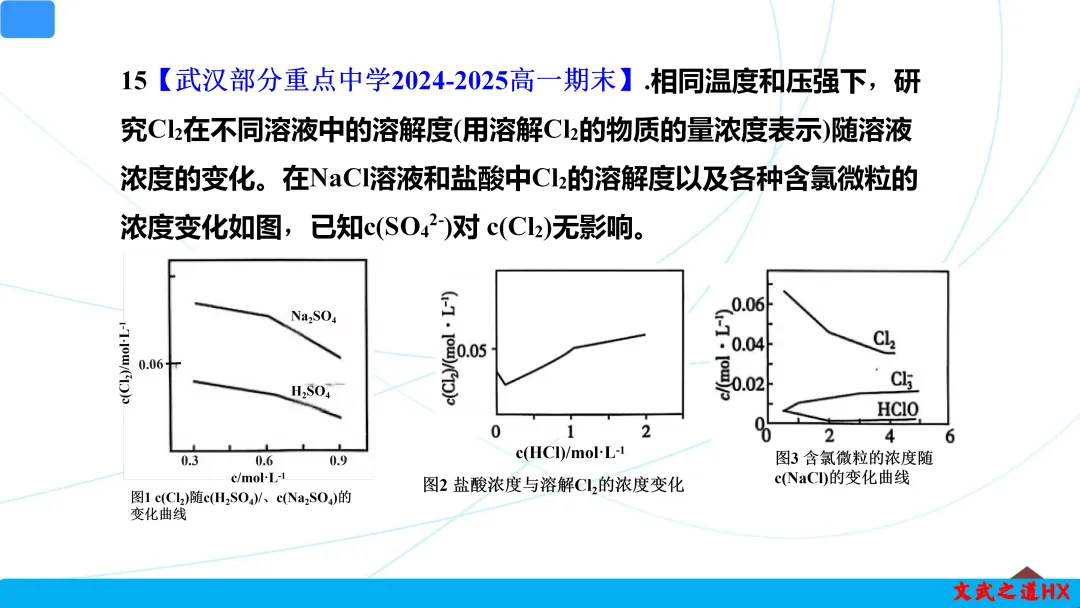
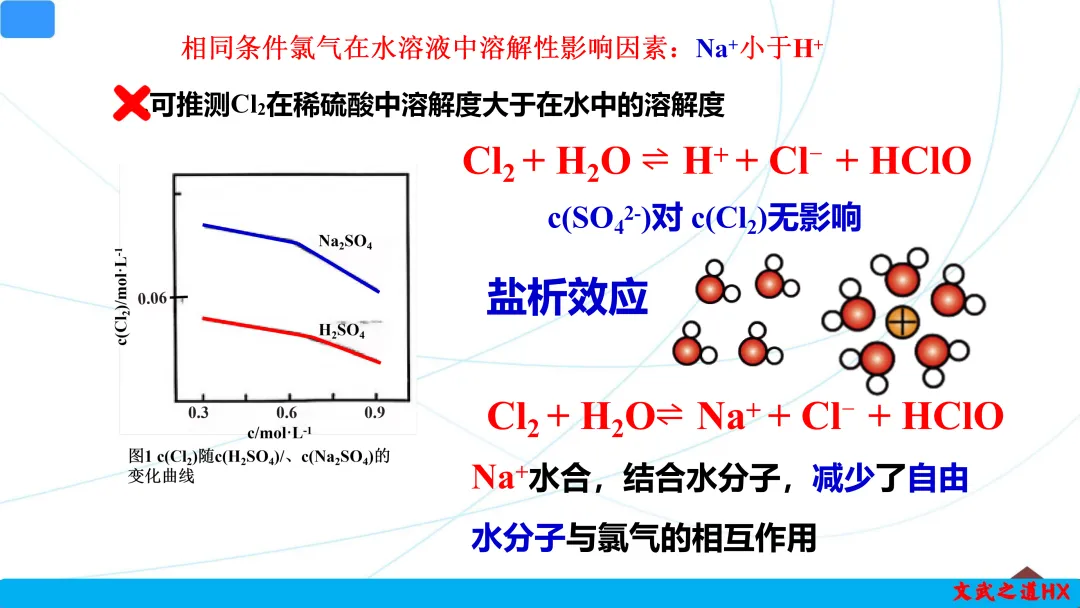
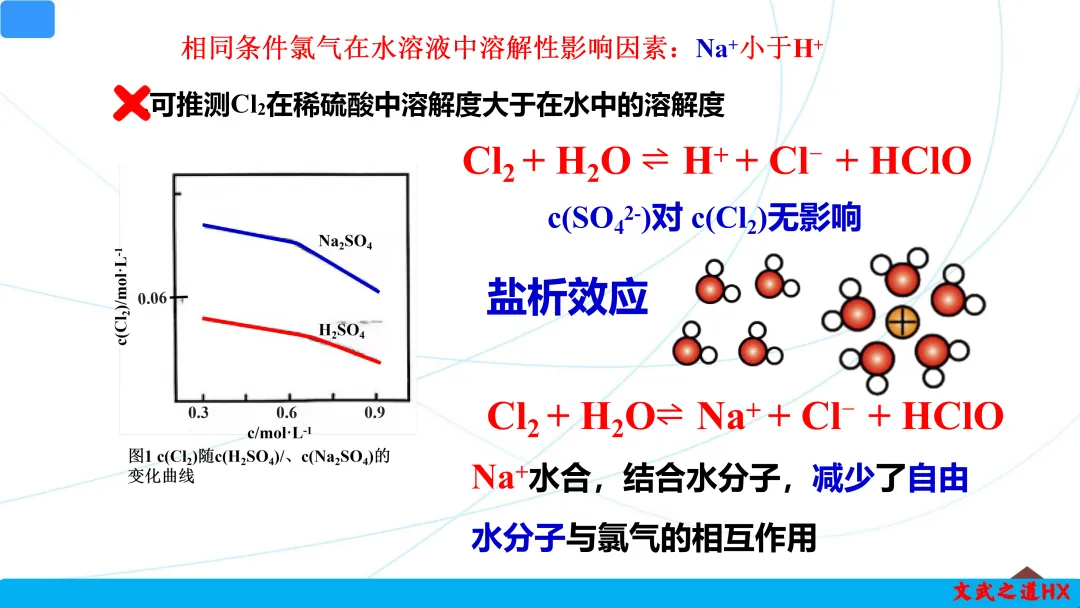
4.【武汉部分重点中学2024-2025高一期末15】.相同温度和压强下,研究Cl2在不同溶液中的溶解度(用溶解Cl2的物质的量浓度表示)随溶液浓度的变化。在NaCl溶液和盐酸中Cl2的溶解度以及各种含氯微粒的浓度变化如图,已知c(SO42-)对 c(Cl2)无影响。
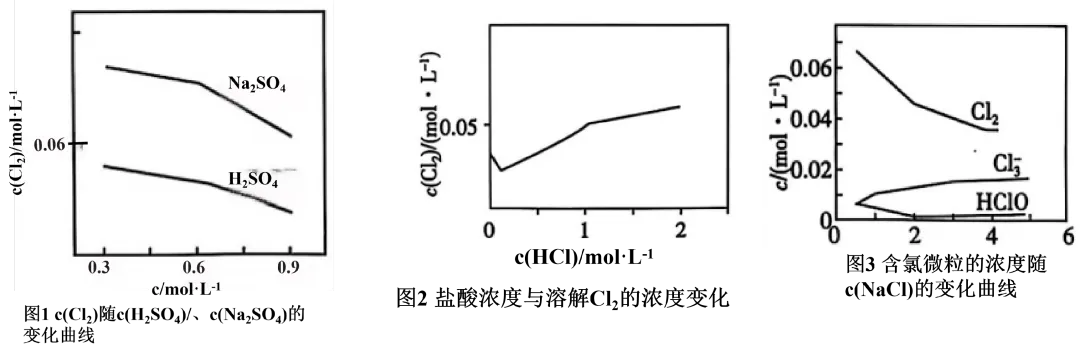
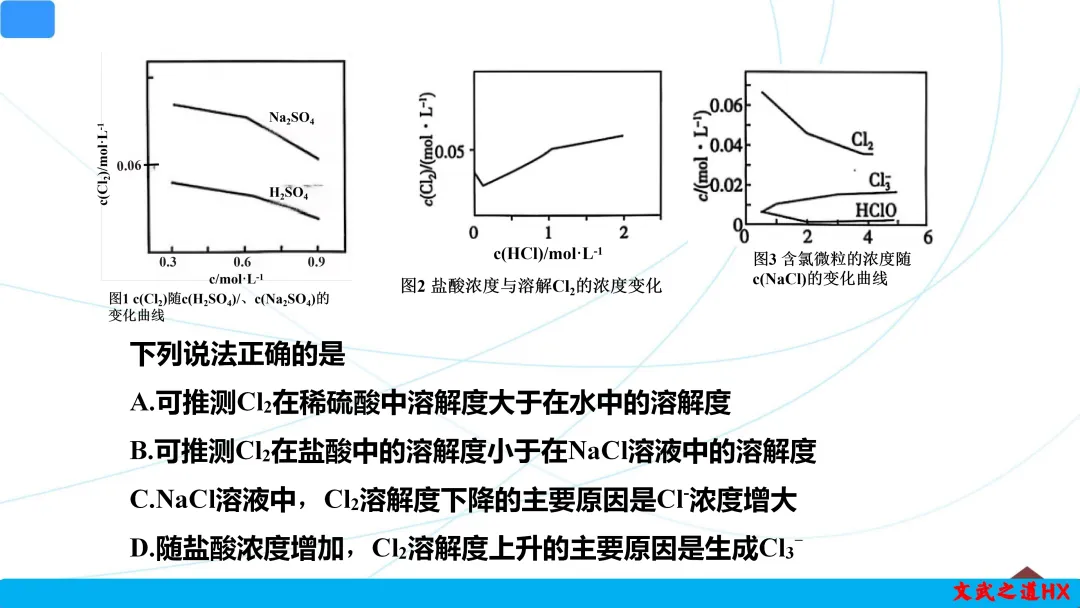
下列说法正确的是
A.可推测Cl2在稀硫酸中溶解度大于在水中的溶解度
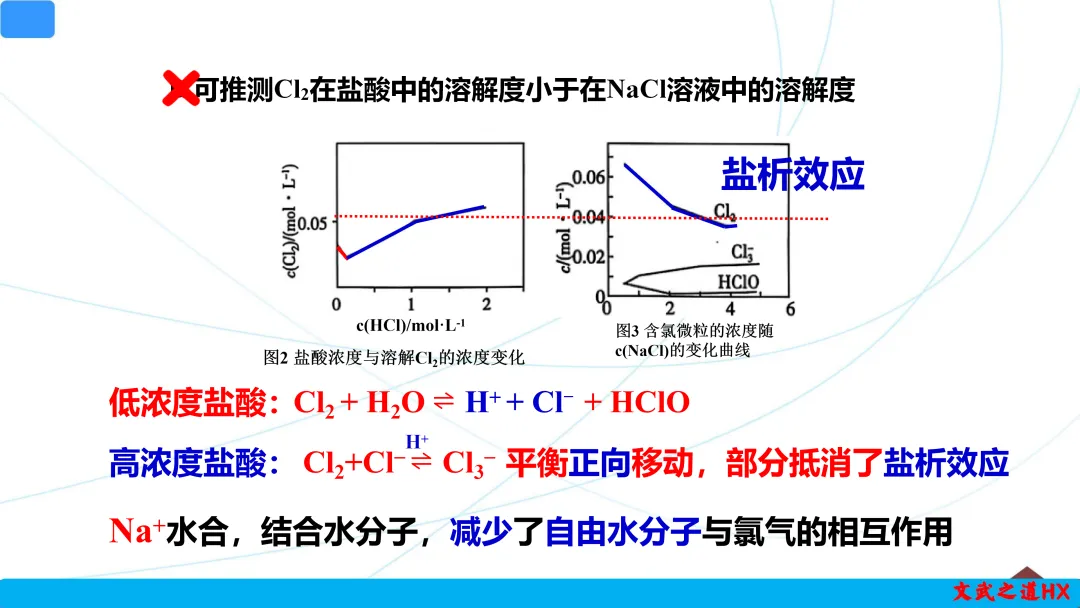
B.可推测Cl2在盐酸中的溶解度小于在NaCl溶液中的溶解度
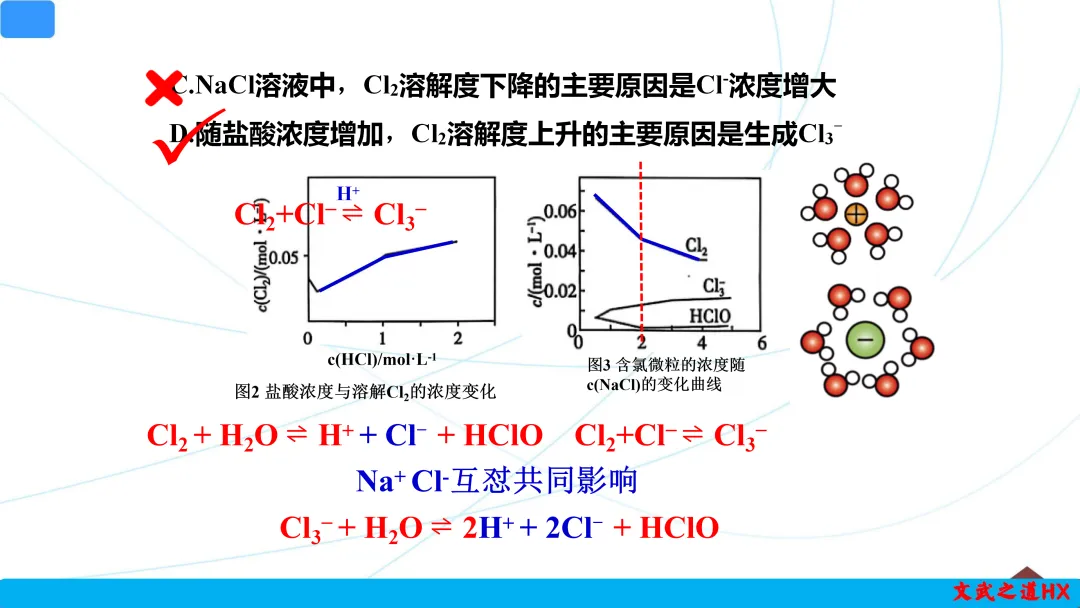
C.NaCl溶液中,Cl2溶解度下降的主要原因是Cl-浓度增大
D.随盐酸浓度增加,Cl2溶解度上升的主要原因是生成Cl3-
理论解释:
氯气在溶液中氯气在溶液中的行为较为复杂,受多种因素影响,以下是主要情况:
1. 氯气在水中的溶解与反应
氯气在水中溶解度较小,1体积水约溶解2体积氯气(标准状况下)。
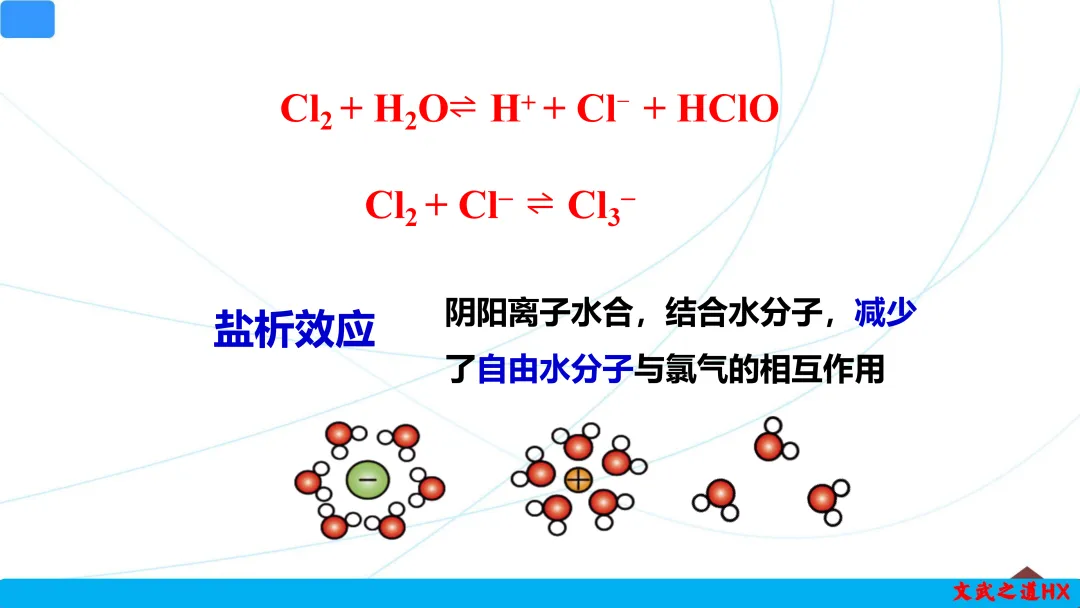
溶解的氯气部分与水发生可逆反应:Cl2+H2O⇌HCl+HClO,生成盐酸和次氯酸。次氯酸具有强氧化性,是氯水具有漂白、消毒作用的原因。
溶液中还存在另一个平衡:Cl2+Cl−⇌Cl3−,但该平衡在纯水中进行程度较小。
2. 氯气在不同溶液中的溶解度变化
在盐酸溶液中:
低浓度盐酸(HCl浓度<0.2 kmol/m³)时,氯气溶解度随HCl浓度增加而急剧下降,因为H+、Cl−抑制了Cl2与水的反应(平衡Cl2+H2O⇌HCl+HClO逆向移动)。
高浓度盐酸(HCl浓度>0.2 kmol/m³)时,溶解度轻微上升,因为Cl−浓度增大促进了Cl2+Cl−⇌Cl3−平衡正向移动,部分抵消了盐析效应。
在金属氯化物溶液中:
如NaCl、KCl、MgCl2等溶液,随着氯化物浓度增加,氯气溶解度显著下降,主要原因是“盐析效应”——金属离子水合数较高,结合水分子能力强,减少了自由水分子与氯气的相互作用,导致氯气溶解度降低。
对于ZnCl2等溶液,由于Zn2+易形成氯络合物,降低了自由Zn2+浓度,对氯气溶解度的抑制作用相对较弱。
在非氯化物盐溶液中(如Na2SO4):氯气溶解度也随盐浓度增加而减小,说明盐析效应是普遍存在的,且非氯化物盐的盐析效应与氯化物盐类似,但无Cl−对平衡的促进作用。
3. 实际应用中的意义
实验室制取氯气时:常用排饱和食盐水法收集氯气,利用饱和食盐水中高浓度Cl−和盐析效应,降低氯气在水中的溶解度,减少氯气损失。
工业上处理含氯废水或废气时:需考虑溶液中离子浓度、酸碱度等因素对氯气溶解度的影响,通过调节条件控制氯气的溶解和反应,以达到净化或回收的目的。
综上,氯气在溶液中的溶解和反应受水解平衡、氯离子浓度、盐析效应等多种因素共同影响,需综合考虑这些因素才能准确理解和应用氯气在溶液中的行为。
PPT展示

通过网盘分享的文件:氯气在水溶液的影响因素的探究
链接: https://pan.baidu.com/s/1kJ86I1w6Ub9jp5B81eB8Kg?pwd=2025 提取码: 2025
--来自百度网盘超级会员v8的分享
资源下载:
我用夸克网盘给你分享了「57.构建“三段四线”模型 突破工艺流程题.pptx」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~4d053A2Sl2~:/
链接:https://pan.quark.cn/s/cc0004fc5e55
01.我用夸克网盘给你分享了「每日一题01」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~b46a3A2TBN~:/
链接:https://pan.quark.cn/s/2faa71e691ce
02.我用夸克网盘给你分享了「每日一题02」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~00313A3BaR~:/
链接:https://pan.quark.cn/s/805466c5fd76
03.我用夸克网盘给你分享了「每日一题03」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~51da3A3m8A~:/
链接:https://pan.quark.cn/s/b5f158b39a6d
04.我用夸克网盘给你分享了「每日一题04」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~facb3A4jsE~:/
链接:https://pan.quark.cn/s/496c695a80fa
05.我用夸克网盘给你分享了「每日一题05」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~74203A5fxu~:/
链接:https://pan.quark.cn/s/4a71f6b7d1ed
06.我用夸克网盘给你分享了「每日一题06」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~c82f3A6ZtL~:/
链接:https://pan.quark.cn/s/77eeb6722a13
07.我用夸克网盘给你分享了「每日一题07」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~76163A7YMq~:/
链接:https://pan.quark.cn/s/529c96396243
08.我用夸克网盘给你分享了「每日一题08」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~9f643A8fIF~:/
链接:https://pan.quark.cn/s/750b7be5151d
09.我用夸克网盘给你分享了「每日一题09」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~29cf3A9uT2~:/
链接:https://pan.quark.cn/s/25eb6e1cd53e
10.我用夸克网盘给你分享了「每日一题10」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~c0393ABn7v~:/
链接:https://pan.quark.cn/s/5ad64f2258bb
11.我用夸克网盘分享了「每日一题11」,点击链接即可保存。打开「夸克APP」,无需下载在线播放视频,畅享原画5倍速,支持电视投屏。
链接:https://pan.quark.cn/s/571e4f3628c0
12.我用夸克网盘给你分享了「每日一题12」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~4f7b3AChnN~:/
链接:https://pan.quark.cn/s/abd1323e9393
13.我用夸克网盘给你分享了「每日一题13」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~6fbc3AE094~:/
链接:https://pan.quark.cn/s/fc23d644a681
14.我用夸克网盘给你分享了「每日一题14」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~5d233AF2sN~:/
链接:https://pan.quark.cn/s/e533c63cbefb
15.我用夸克网盘给你分享了「每日一题15」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~fd583AGo1a~:/
链接:https://pan.quark.cn/s/0d6b5fa31885
更多资源:

高考真题链接:
更多个人资源请点击下图

个人资源请进微店了解
 |  |
喜欢作者是对作者最大的支持 下载资料同时,若感觉资料合用记得 关注,点赞,分享,收藏
