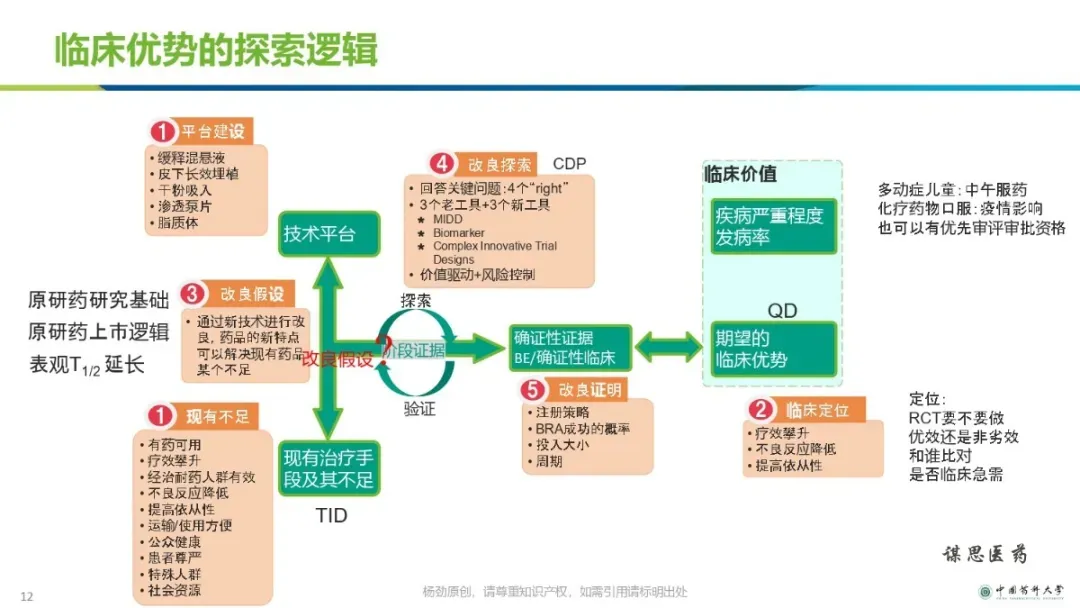
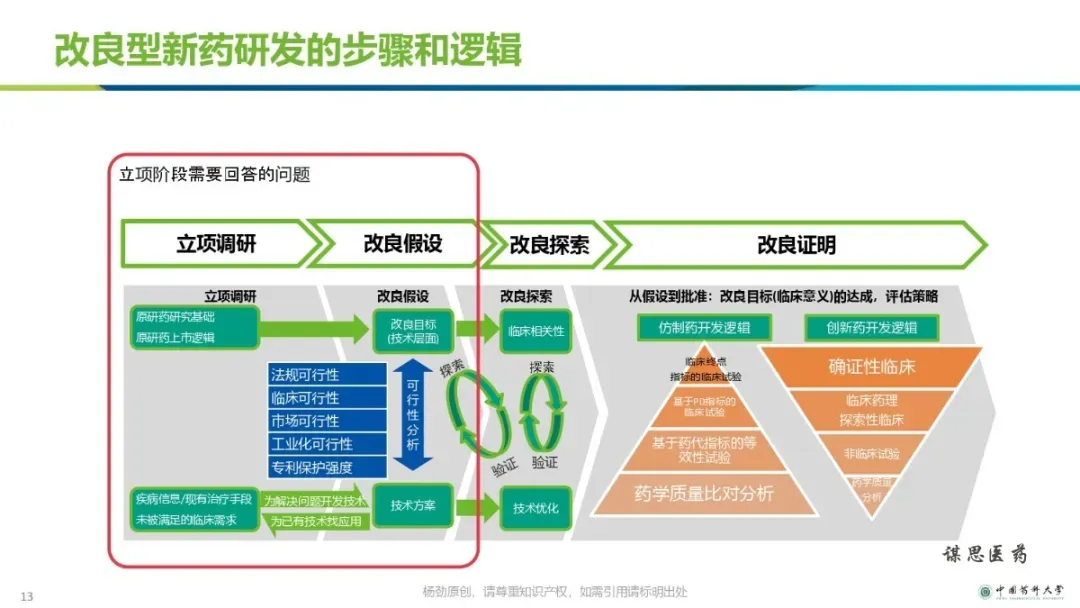
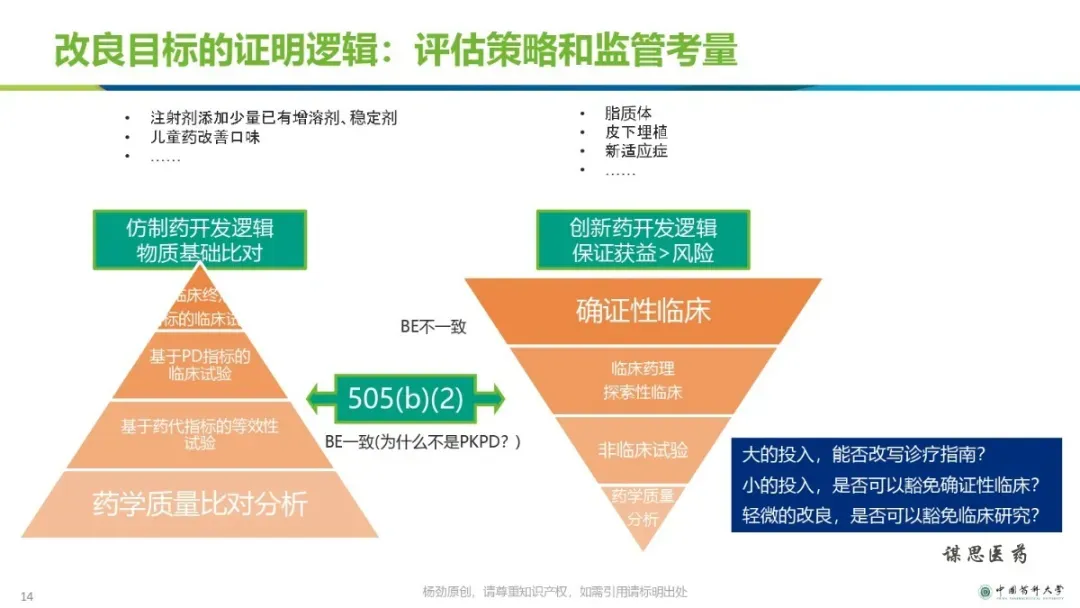
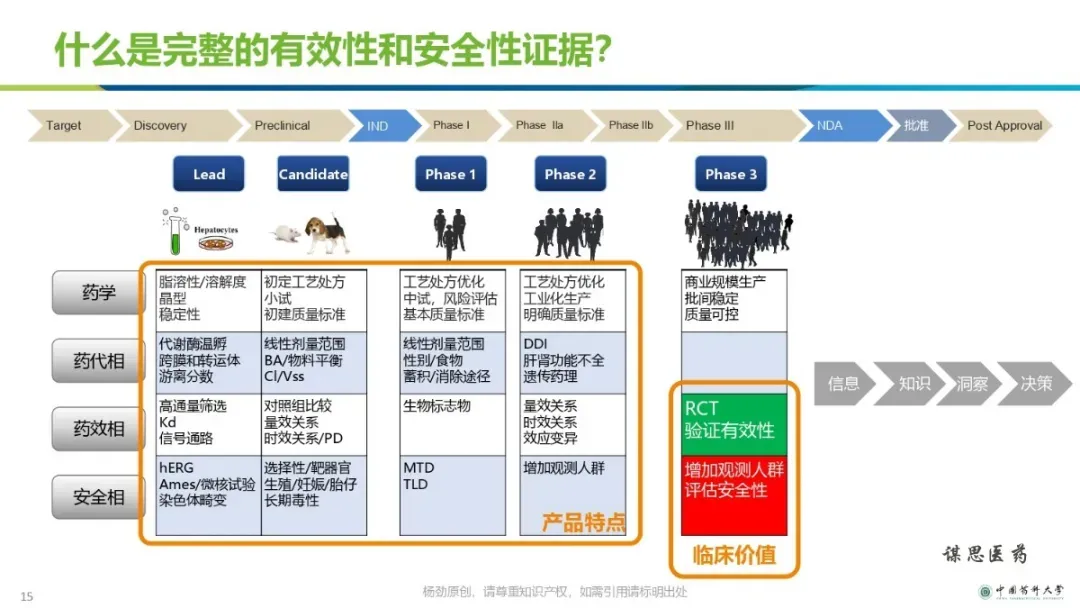
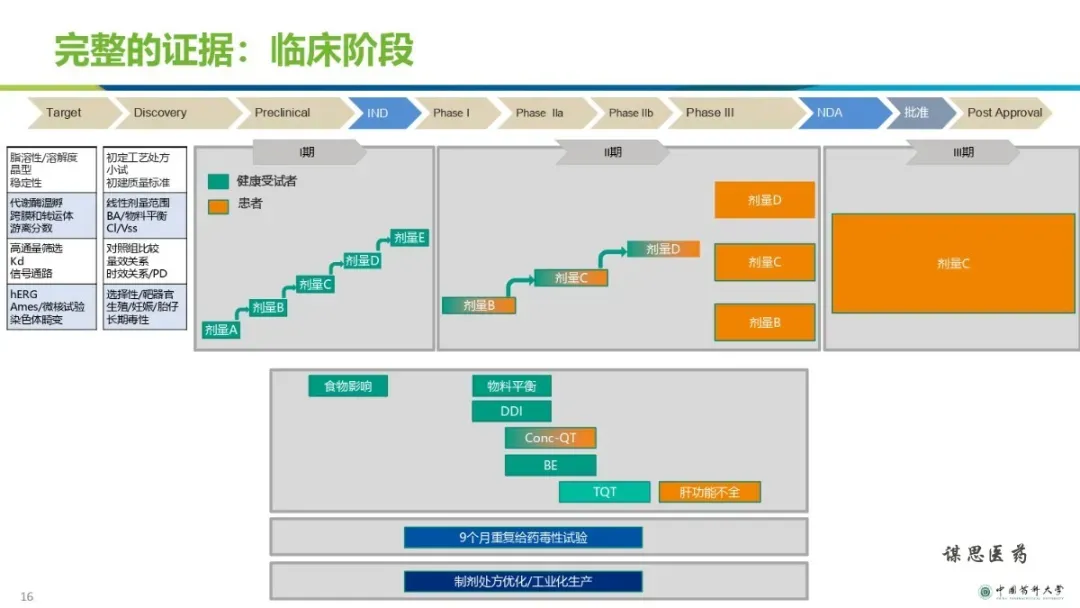
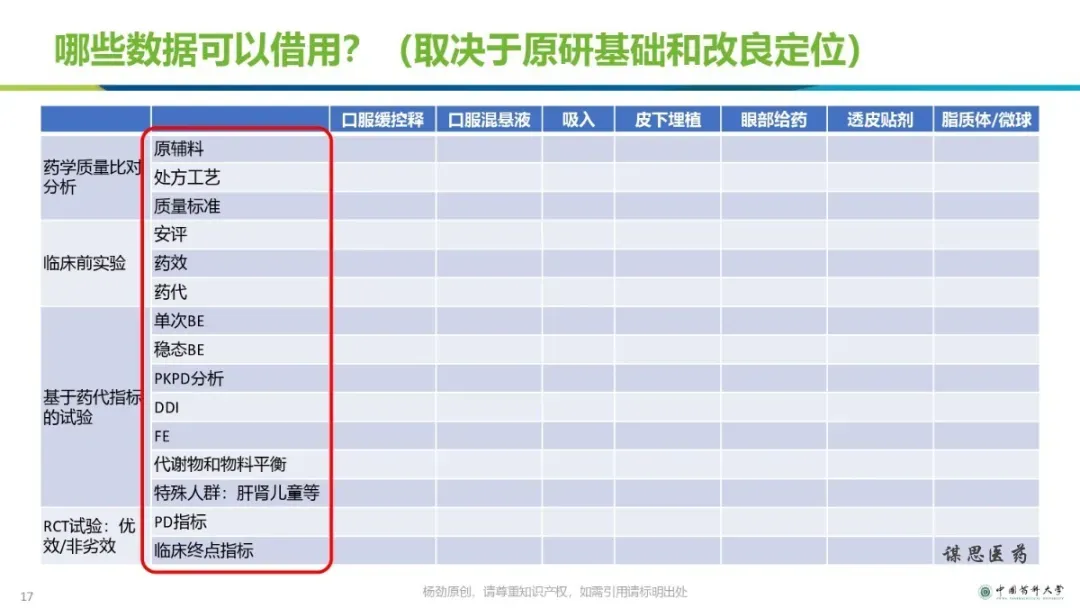
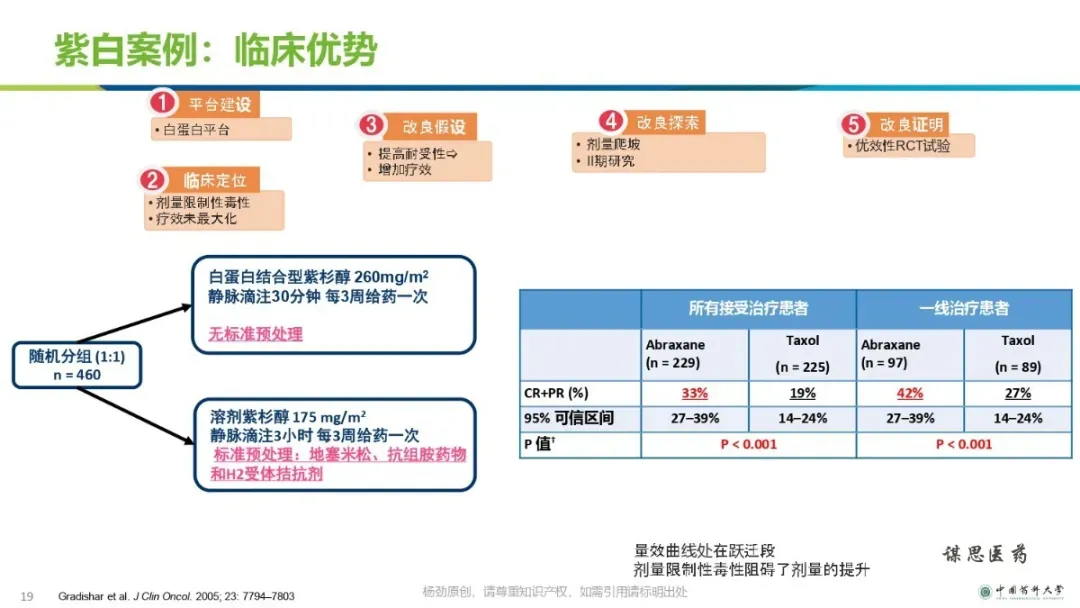
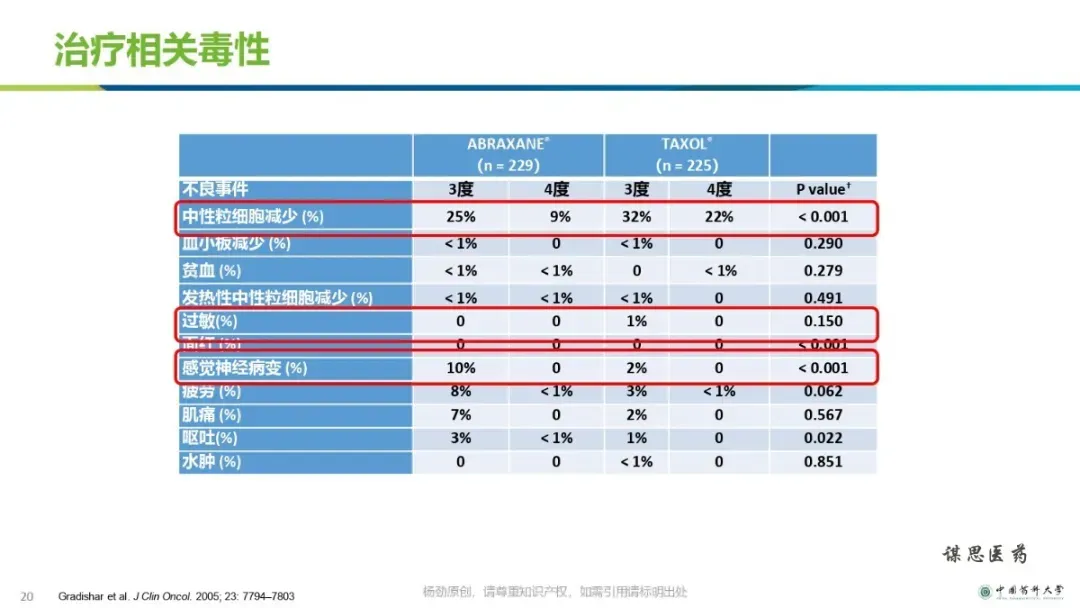
改良型新药的立项和研发策略【ppt】
- 2026-05-22 10:39:14






















文章信息源于网络,登载该文章目的为更广泛的传递行业信息,不代表赞同其观点或对其真实性负责。文章版权归原作者及原出处所有,文章内容仅供参考。本网拥有对此声明的最终解释权,若无意侵犯版权,请联系小编删除。
新法规环境下药品技术转移策略与实施操作研讨班
时间:2026年03月19日-21日
地点:南京市+腾讯会议
课程背景与目标
课程时间安排
03月20日 9:00-12:00 13:30-16:30
一、国家药监局2025年第134号公告深度解读
1.技术转移相关核心条款解析:
a重点讲解公告中关于强化技术转移管理的具体条款(第一、(四)条),明确受托生产企业的核心责任
b受托生产企业在技术转移中的评估义务、风险防控要求、质量管理体系衔接要求。
c技术转移失败或不足所引发的法律后果与质量责任
2.委托生产许可程序与技术转移的衔接要求:跨省委托“先B后C”原则对技术转移的影响与应对。
3.高风险产品(无菌药品、中药注射剂等)技术转移的特殊监管要求。
二、药品技术转移全流程管理实操要点
1.技术转移前的评估与准备:
a受托方对持有人的评估:如何评估持有人的质量管理能力与技术转移方案的可行性。
b持有人对受托方的评估:指导持有人如何现场考核受托方的厂房设施、设备能力及质量管理体系。
2.技术转移项目组建与职责分工:项目组构成(转移方、接收方、质量管理部门、设备部门等)、各方职责与协同机制。
3.技术转移文件体系构建:转移文件目录(工艺规程、批生产记录、质量标准、检验方法等)、文件审核与归档要求。
4.技术转移方案的设计与执行
a制定技术转移方案:包括工艺规程、关键工艺参数、中间控制点、质量对比研究等核心内容的转移计划。
b确认与验证工作:详细讲解设施设备、清洁方法、分析方法、生产工艺的确认或验证要求。
5.关键环节实操要点
a共线生产风险评估:如何在技术转移中开展并记录共线生产风险评估,以及如何根据评估结论采取风险控制措施
b数据与记录管理:数据汇总分析、验收标准、转移报告审核要点,确保转移前后产品质量一致,并配合持有人完成技术转移报告
主讲人:孙老师 独立咨询师资深专家,(WHO)TB FDC技术顾问。曾在西安杨森、德国汉姆等公司从事药品注册和国际医药法规咨询。曾参与NMPA国际GMP对比调研报告和GMP内部审计系列模板的起草。熟悉欧美注册认证等法规。多家咨询公司制药法规高级咨询师,国家药监局顾问。03月21日 9:00-12:00 13:30-16:30
一、技术转移中的质量风险防控与合规管理
1.技术转移各环节风险识别与控制:软硬件条件差异、工艺偏差、变更管理等风险点梳理与防控措施。
2.留样与稳定性考察的衔接管理:委托双方留样责任划分、重大偏差与重大变更后稳定性考察要求。
3.技术转移中的变更控制:变更类别判定、审批程序与持有人的协同管理要求。
4.质量信息沟通机制构建:偏差、超标/超趋势、验证结果等关键信息的沟通清单、时限与责任划分。
5.知识产权保护与技术秘密管理:技术转移过程中商业秘密与技术信息的保护措施。
二、药品技术转移项目管理流程解析
1.如何建立技术转移合规性体系与案例
2.技术转移工作和公司质量管理、工程管理等内容如何关联案例?
3.如何协调各部门人员的参与度案例?
4.技术转移过程包括哪些具体活动?
5.各项活动的具体工作内容和用途是什么案例?
三、技术转移过程中常见问题的剖析和解答
1.转出方和接收方对技术转移的成功标准认知不一致
2.技术转移过程中缺乏规范化管理
3.转出方和接收方对技术转移过程中的关键技术问题认知不足
4.技术转移头对头对比研究对数据完整性的要求
5.技术转移或新产品引入风险评估的评价要求;
6.人/机/料/法/环/测六个方面的技术转移评估案例分享;
7.技术转移/工艺验证/清洁验证三者的关系与控制策略与案例;
8.技术转移中涉及产品共线生产对清洁验证的要求与对策
主讲人:刘老师 国内知名的GMP专家 体系专家 医药工程高级工程师。负责药物研发、注册质量管理体系构建与监管。拥有30 余年研发、生产、GMP管理经验,曾经在国内多家药企担任生产、质量的高管等各管理岗位,主导参与建设多条生产线,亲自参加多次FDA、WHO、TGA和CEP认证及国内检查会务费
线下培训费:4800元/单位,每单位限额3人(1600元/人),包含(专家费、资料费、场地费、现场问答等)。食宿统一安排,费用自理。
线上费用:4000元每单位(会务费包括:发票、培训、答疑、电子版资料视频回放等),可投屏全员观看,可满足同集团不同厂区同时观看,堪比内训效果!
报名咨询
1. 移动端直接扫描/识别下图二维码即可在线报名
2. 联系咨询
报名咨询:王老师 13261834175
报名邮箱:3303567772@qq.com;
微信咨询:w13261834175
3. 移动端直接扫描/识别下图二维码微信在线咨询

近期精品专修班汇总
地点 时间 (点击↓链接阅读全文) 线上 1月30日 《清洁验证技术指南》深度解读与实操落地 南京+线上
3月19-21日 新法规环境下药品技术转移策略 南京 3月27-29日 药物质量研究分析方法的高效建立及典型案例分享 线上 3月21-22日 南美、西亚、中东及非洲国家药品注册策略和流程 线上 3月21-22日 小核酸药物非临床研究策略专题 线上 3月28-29日 MAH制度下半场如何推进《关于加强药品受托生产监督管理工作的公告》执行 直播 3月28-29日 从合规到卓越——GLP专题负责人核心能力进阶提升研修班 线上直播 3月28-29日 疫苗从IND到BLA全生命周期研发注册(中美欧)实操培训班 线上直播 3月28-29日 2026实验设计(DOE)赋能重组蛋白工艺开发与优化培训班 直播 3月28-29日 生物制药国内外审计策略及迎检实战指导与GMP现场检查重点专题研讨班 线上 3月28-29日 细胞基因治疗产品质量与工艺在临床转化准备与实施 200期回放 近两年特价课 可购买往期培训视频回播 联系方式
扫码添加微信
电话微信|王妍:13261834175
咨询注明|公司+姓名+职位+电话
Science Technology
提供制药企业|相关单位|内训服务
诚邀赞助单位|协办单位及新产品|新设备展示单位



